Thai FDA - NMPA (China)
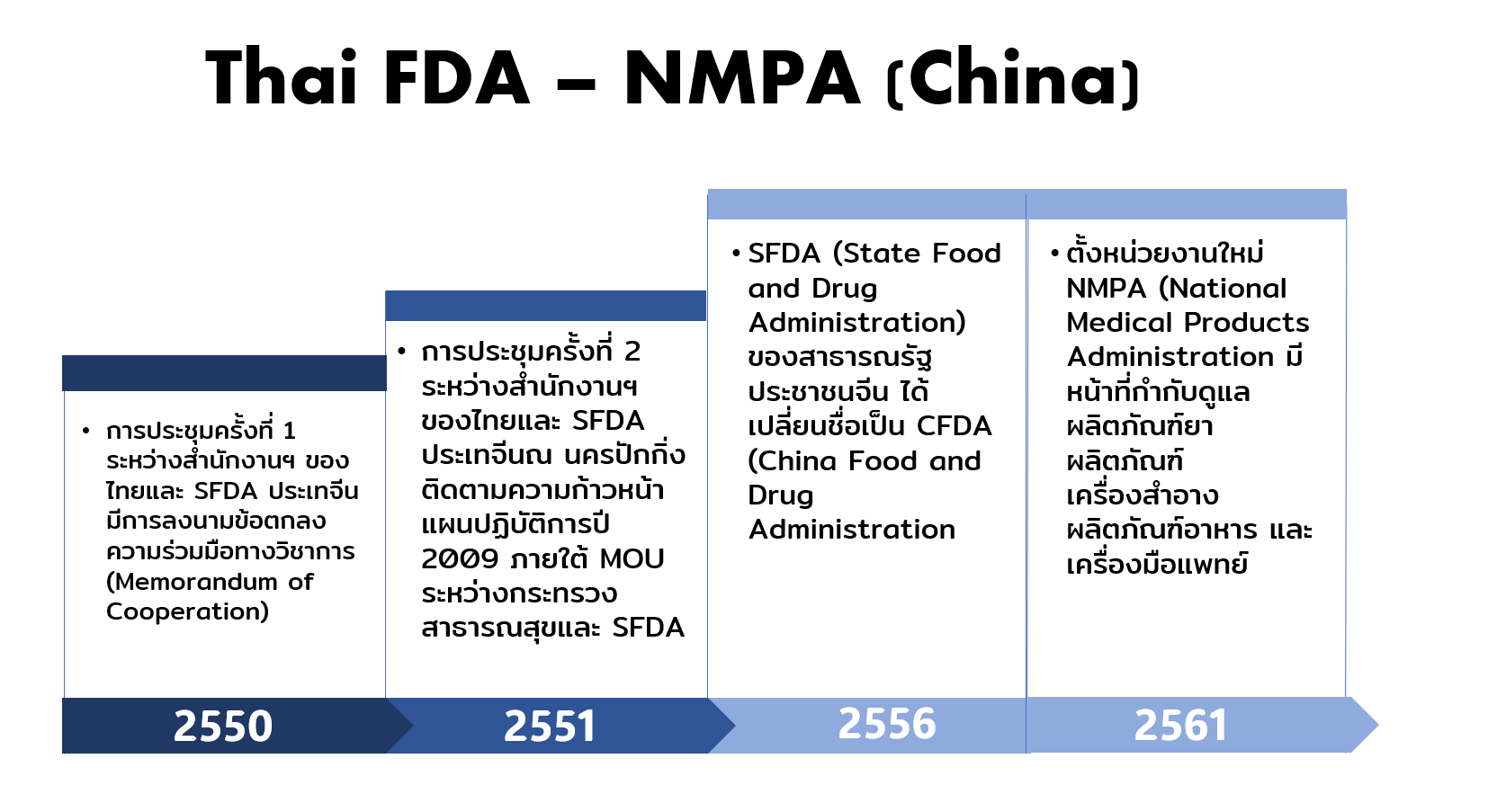
กระทรวงสาธารณสุขและ SFDA ของสาธารณรัฐประชาชนจีน ได้ลงนามข้อตกลงความร่วมมือทางวิชาการ (Memorandum of Cooperation) เมื่อวันที่ 18 มกราคม 2550 มีสาระสำคัญคือ การแลกเปลี่ยนข้อมูล ความร่วมมือทางวิชาการระหว่างทั้ง 2 ประเทศ และจากการเจรจาหารือร่วมกับ SFDA 2 ครั้ง เมื่อวันที่ 28-30 พฤษภาคม 2550 และ 6 กันยายน 2550 ณ ประเทศสาธารณรัฐประชาชนจีน มีความเห็นพ้องกันว่าให้จัดทำ Plan of action โดยจัดประชุม Joint Working Committee ระหว่าง 2 หน่วยงานขึ้น ในปี 2556 SFDA (State Food and Drug Administration) ของสาธารณรัฐประชาชนจีน ได้เปลี่ยนชื่อเป็น CFDA (China Food and Drug Administration) โดยมีภารกิจกำกับดูแลความปลอดภัยของผลิตภัณฑ์ 4 ประเภท ได้แก่ ผลิตภัณฑ์ยา ผลิตภัณฑ์เครื่องสำอาง ผลิตภัณฑ์อาหาร และเครื่องมือแพทย์ ต่อมาในปี 2561 ได้มีการแบ่งหน้าที่และตั้งหน่วยงานใหม่ คือ NMPA (National Medical Products Administration) ที่มีหน้าที่กำกับดูแลผลิตภัณฑ์ยา ผลิตภัณฑ์เครื่องสำอาง ผลิตภัณฑ์อาหาร และเครื่องมือแพทย์ โดยที่ CFDA ยังคงมีหน้าที่กำกับดูแลผลิตภัณฑ์อาหาร
สำนักงานคณะกรรมการอาหารและยาเป็นเจ้าภาพจัดการประชุม The 1st Joint Working Committee Meeting of the Ministry of Public Health of Thailand and the State Food and Drug Administration of the People’s Republic of China ที่ State Food and Drug Administration (SFDA) ระหว่างวันที่ 26-27 ธันวาคม 2550 โดยมีวัตถุประสงค์เพื่อจัดทำแผนปฏิบัติงานรองรับความร่วมมือดังกล่าว ซึ่ง SFDA ได้มอบหมาย Mr. Wu Zhen Deputy Commissioner, SFDA เป็นหัวหน้าคณะมาพร้อมคณะทำงานอีก 7 ท่าน และได้มีการลงนามแผนปฏิบัติการร่วมกัน โดยฝ่ายไทยมีนายแพทย์ มรกต กรเกษม รัฐมนตรีช่วยว่ากระทรวงสาธารณสุขเป็นผู้ลงนาม นอกจากนั้นผู้เชี่ยวชาญจาก SFDAได้มาบรรยายด้านกฎระเบียบและข้อกำหนดการขึ้นทะเบียนตำรับยาแผนโบราณ เป็นประโยชน์แก่ผู้ประกอบการ และเจ้าหน้าที่ฝ่ายไทย ซึ่งเข้ารับฟังจำนวน 129 คน รวมถึงเจ้าหน้าที่ฝ่ายไทยนำคณะจีนศึกษาดูงานโรงงานผลิตยาสตรีเพ็ญภาคในส่วนของสถานที่เก็บวัตถุดิบ ขั้นตอนการผลิต และขั้นตอนการบรรจุ จำนวนรวมทั้งสิ้น 23 ราย
ในปี พ.ศ. 2551 สำนักงานคณะกรรมการอาหารและยาได้มีการดำเนินงานตาม MOU ระหว่างกระทรวงสาธารณสุขและ SFDA คือการเข้าร่วมประชุม The 2nd Joint Working Committee Meeting of the Ministry of Public Health of Thailand and the State Food and Drug Administration of the People’s Republic of China ที่ State Food and Drug Administration (SFDA) ณ กรุงปักกิ่ง สาธารณรัฐประชาชนจีน ระหว่างวันที่ 24-26 สิงหาคม 2552 มีวัตถุประสงค์เพื่อติดตามความก้าวหน้าแผนปฏิบัติการปี 2009 ภายใต้ MOU ระหว่างกระทรวงสาธารณสุขและ SFDA
ประเด็นความร่วมมือ
1. การแลกเปลี่ยนข้อมูลด้านกฎระเบียบ ที่เป็นภาษาอังกฤษบนเว็บไซต์
2. การแลกเปลี่ยนบุคลากร ด้านการควบคุมยาจีนแผนโบราณ ด้าน Compulsory licensing และด้านเครื่องมือแพทย์
3. การตรวจสอบยาอย่างง่าย โดยเทคโนโลยี NIR
4. การพัฒนาศักยภาพบุคลากร ด้านเครื่องมือแพทย์ การกำกับดูแลชีววัตถุ และการควบคุม และระบบป้องกันคุณภาพ
ของยาจีนแผนโบราณ
5. การสร้างระบบเตือนภัยผลิตภัณฑ์สุขภาพ
5.1 การสร้างระบบเตือนภัยเร่งด่วนด้านความปลอดภัยและคุณภาพของผลิตภัณฑ์สุขภาพภายหลังออกสู่ท้องตลาด
5.2 ศึกษาดูงานเพื่อพัฒนาศักยภาพบุคลากรด้านการเฝ้าระวังความปลอดภัยจากการใช้ยา
วัตถุประสงค์
1. เพิ่มความร่วมมือและความสัมพันธ์ระหว่างหน่วยงานของทั้ง 2 ประเทศ
2. เสริมสร้างความเข้มแข็งการสนับสนุนคุณภาพและความปลอดภัยของผลิตภัณฑ์ยาและเครื่องมือแพทย์
3. เพิ่มความเข้าใจซึ่งกันและกันระหว่าง 2 หน่วยงานทางด้านกฎระเบียบทางเทคนิค มาตรฐาน และขั้นตอนการประเมินความสอดคล้อง
4. แลกเปลี่ยนประสบการณ์ทางด้าน compulsory licensing
ประเด็นที่เกี่ยวข้องกับ อย.
นายแพทย์พิพัฒน์ ยิ่งเสรี เลขาธิการคณะกรรมการอาหารและยาเป็นหัวหน้าคณะฝ่ายไทยเข้าเยี่ยม คารวะ Mr. Shao Mingli Commissioner SFDA และประชุมหารือเพื่อติดตามความก้าวหน้าแผนปฏิบัติการปีพ.ศ. 2552 กับเจ้าหน้าที่ SFDA ซึ่งมี Mr.Wu Zhen Deputy Commissioner SFDA เป็นหัวหน้าคณะ ซึ่งแผนปฏิบัติการปีพ.ศ. 2552 ครอบคลุมงาน 7 ด้าน โดยการสร้างระบบเตือนภัยผลิตภัณฑ์สุขภาพเป็นกิจกรรมที่เพิ่มใหม่ ความคืบหน้าของแผนปฏิบัติการ สาระสำคัญที่ 2 ฝ่ายตกลงกันคือ
1. การแลกเปลี่ยนข้อมูลกฎระเบียบ : ยาแผนปัจจุบัน ยาแผนโบราณ และเครื่องมือแพทย์ โดยทั้ง 2 ฝ่ายพร้อมที่จะแลกเปลี่ยนข้อมูลที่มีอยู่ในปัจจุบันและเตรียมแปลกฎหมายเป็นภาษาอังกฤษเพิ่มเติมเพื่อที่จะแลกเปลี่ยนกันในอนาคต
2. จัดประชุมเจ้าหน้าที่และผู้เชี่ยวชาญ : เครื่องมือแพทย์ และ Compulsory Licensing โดยฝ่ายไทยต้องการจัดประชุมบรรยายโดยผู้เชี่ยวชาญด้านเครื่องมือแพทย์ และฝ่ายจีนต้องการทราบประสบการณ์การทำ CL ของไทย โดยทั้ง 2 ฝ่ายยินดีที่จะแลกเปลี่ยนผู้เชี่ยวชาญกัน
3. จัดฝึกอบรม : การตรวจสอบยาอย่างง่ายโดยเทคโนโลยี NIR และยาจีนแผนโบราณ โดยฝ่ายไทยต้องการให้ฝ่ายจีนถ่ายทอดความรู้และประสบการณ์การใช้เครื่อง NIR ข้อมูลยา (library) และ ประสบการณ์ด้านการพัฒนาและการควบคุมการผลิตยาจีนแผนโบราณ โดยจีนยินดีให้ข้อมูลและให้ความช่วยเหลือ
4. ศึกษาดูงาน : ชีววัตถุ เครื่องมือแพทย์ เครื่องมือแพทย์แผนจีน และระบบเตือนภัยผลิตภัณฑ์สุขภาพ โดยฝ่ายไทยต้องการศึกษาดูงานที่ประเทศจีน ซึ่งจีนยินดีต้อนรับทีมงานของไทยด้านเครื่องมือแพทย์แผนจีน และระบบเตือนภัยผลิตภัณฑ์สุขภาพ

